Isaura Beatriz Borges Silva
Orientadora: Profa. Dra. Mari Cleide Sogayar
Pesquisadores Colaboradores: Ana Cláudia Oliveira Carreira; Milton Yutaka Nishiyama Junior; Fernando Janczur Velloso; Fernando Henrique Lojudice; Camila Harumi Kimura.
Possui graduação em Biotecnologia pela Universidade Federal de Uberlândia (2017), Mestrado em Biotecnologia pelo Instituto de Ciências Biomédicas da Universidade de São Paulo (2019) e, atualmente, é aluna de Doutorado em Bioquímica pelo Instituto de Química da Universidade de São Paulo. Atua no Grupo NUCEL desenvolvendo o Projeto de Doutorado intitulado: “Caracterização do transcritoma de células-tronco embrionárias durante sua diferenciação em células produtoras de insulina na ausência e na presença de fatores peptídicos de crescimento/diferenciação” e, também, atua no Projeto de “Encapsulamento de ilhotas pancreáticas visando à terapia do Diabetes mellitus tipo 1 insulina-dependente” sob orientação da Profa. Dra. Mari Cleide Sogayar. Possui experiência nas áreas de Biologia Celular e Molecular, Genética e Virologia.
Diabetes mellitus insulino-dependente (T1D): Bases moleculares e Terapia Celular – Projeto Temático 2016/05311-2.
O diabetes mellitus (DM) é uma doença crônica caracterizada pela ausência da produção de insulina (DM1) ou ineficiência na sua utilização pelo indivíduo (DM2). Consequentemente, pacientes portadores de DM desenvolvem um quadro de hiperglicemia, o qual, se não for controlado, pode desencadear sérias complicações no funcionamento de órgãos vitais (DIABETES CONTROL AND COMPLICATIONS TRIALS RESEARCH GROUP – DCCT, 1993). Os tratamentos convencionais do DM1, na maioria das vezes, não são capazes de manter o perfeito controle dos níveis glicêmicos (DCCT, 1997). Os riscos cirúrgicos inerentes ao transplante de pâncreas órgão total estimularam o desenvolvimento de procedimentos menos invasivo em que se realiza o transplante das ilhotas pancreáticas. O transplante de ilhotas pancreáticas vem sendo uma das estratégias estudadas como terapia celular para esta doença, inclusive por nosso grupo de pesquisa, que introduziu esta tecnologia no Brasil (ELIASCHEWITZ et al, 2004). Entretanto, um ponto limitante aos protocolos de transplante de ilhotas para a reversão do DM1 é a baixa disponibilidade de doadores de pâncreas e a manutenção e sobrevivência das ilhotas em cultura após o isolamento. Diante da crescente necessidade de busca por novas intervenções terapêuticas para o DM1, estratégias baseadas na diferenciação de células-tronco em células produtoras de insulina, têm se mostrado uma abordagem promissora para superar a dependência de células β-pancreáticas humanas para o transplante (LOJUDICE; SOGAYAR, 2008). O processo de diferenciação in vitro consiste de etapas consecutivas de tratamentos com citocinas ou moduladores de sinalização, em doses específicas, para ativar ou inibir as principais vias de sinalização que controlam a organogênese pancreática (Figuras 1 e 2).
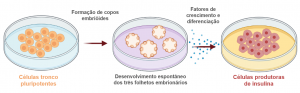
Figura 1: Diferenciação de células-tronco pluripotentes em células produtoras de insulina através da aplicação de fatores de crescimento e diferenciação que participam da organogênese pancreática.
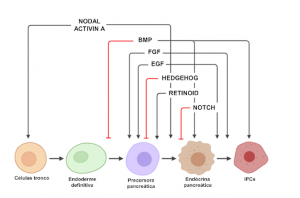
Figura 2: Representação esquemática das vias de sinalização que coordenam cada etapa da diferenciação β-pancreática.
O grupo NUCEL têm buscado o estabelecimento de um protocolo de diferenciação que permita obter células produtoras de insulina funcionais e em grande número (LOJUDICE, 2008; KOSSUGE, 2013; DA SILVA, 2018). Partindo do protocolo estabelecido pelo grupo, o presente projeto tem como objetivo analisar o perfil transcritômico e o papel dos fatores BMP7 e PDGF-BB, produzidos em nosso laboratório, durante o processo de diferenciação de células-tronco embrionárias murinas (mESCs) em células produtoras de insulina (IPCs). A exploração do efeito destes fatores durante a diferenciação in vitro baseia-se no potencial mitogênico associado ao PDGF-BB (CHEN et al., 2011) e na capacidade do BMP-7 de conduzir a diferenciação de células progenitoras não-endócrinas em células endócrinas (KLEIN et al., 2015; QADIR et al., 2018), demonstrando a possibilidade de aplicação desses fatores na expansão e maturação terminal de IPCs. A análise do transcritoma por RNAseq da diferenciação de mESCs em IPCs, vai permitir traçar as vias regulatórias e identificar as moléculas-chave que atuam nos processos de diferenciação. Posteriormente, serão selecionados os transcritos mais relevantes para a realização de intervenções moleculares (superexpressão e/ou nocauteamento gênico), numa abordagem de genômica funcional. Estes experimentos levarão tanto ao aprimoramento da eficiência atingida nos protocolos de diferenciação in vitro, quanto à caracterização de moléculas que certamente poderão abrir novas perspectivas para o tratamento do DM1.
REFERÊNCIAS
CHEN, H. et al. PDGF signalling controls age-dependent proliferation in pancreatic β-cells. Nature, v. 478, n. 7369, p. 349–355, 2011.
DA SILVA, C. L. L. Terapias alternativas para o diabetes mellitus tipo 1: caracterização funcional do gene Txnip na diferenciação β-pancreática e desenvolvimento de biomaterial inovados para microencapsulamento celular. 203 p. Tese (Doutorado em Ciências Biológicas (Bioquímica)) – Instituto de Química, Universidade de São Paulo, São Paulo, 2018.
DIABETES CONTROL AND COMPLICATIONS TRIAL RESEARCH GROUP. Hypoglycemia in the Diabetes Control and Complications Trial. Diabetes, v. 46, n. 2, p. 271-86, 1997.
DIABETES CONTROL AND COMPLICATIONS TRIAL RESEARCH GROUP. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med, v. 329, n. 14, p. 977-86, 1993.
ELIASCHEWITZ, Freddy Goldberg et al. First Brazilian pancreatic islet transplantation in a patient with type 1 diabetes mellitus. Transplantation proceedings, v. 36, n. 4, p. 1117-1118, 2004.
KLEIN, Dagmar et al. BMP-7 induces adult human pancreatic exocrine-to-endocrine conversion. Diabetes, v. 64, n. 12, p. 4123-4134, 2015.
KOSSUGUE, P. M. Diferenciação de células-tronco embrionárias murinas (mESCs) em células produtoras de insulina (IPCs) e caracterização funcional do gene Purkinje Cell Protein 4 (Pcp4) neste processo. Tese (Doutorado em Ciências (Bioquímica) – Instituto de Química, Universidade de São Paulo, São Paulo, 2013.
LOJUDICE, F. H. Identificação de genes diferencialmente expressos durante diferenciação de células-tronco e caracterização de células progenitoras mesenquimais. 173 p. Tese (Doutorado em Ciências Biológicas (Bioquímica)) – Instituto de Química, Universidade de São Paulo, 2008.
LOJUDICE, Fernando Henrique; SOGAYAR, Mari Cleide. Células-tronco no tratamento e cura do diabetes mellitus. Ciência & Saúde Coletiva, v. 13, p. 19-21, 2008.
QADIR, M. M. F. et al. P2RY1/ALK3-expressing cells within the adult human exocrine pancreas are BMP-7 expandable and exhibit progenitor-like characteristics. Cell reports, v. 22, n. 9, p. 2408-2420, 2018.

